| Главная » Статьи » 9 класс » Химия неметаллов |
Фосфор и его соединения
Строение и свойства атомов. Следующий после азота представитель главной подгруппы V группы Периодической системы — элемент-неметалл фосфор Р. Атомы фосфора по сравнению с атомами азота имеют больший радиус, меньшее значение электроотрицательности, а значит, более выраженные восстановительные свойства. Соединения со степенью окисления -3 атома фосфора встречаются реже, чем у азота (только в фосфидах — соединениях фосфора с металлами, например Са3Р2, Nа3Р). Чаще фосфор проявляет в соединениях степень окисления +5. А вот его соединение с водородом — фосфин РН3 — тот редкий случай, когда ковалентная связь между атомами разных элементов неполярна в силу того, что электроотрицательности фосфора и водорода имеют почти одинаковые значения.
Фосфор — простое вещество. Химический элемент фосфор образует несколько аллотропных модификаций. Из них вы уже знаете два простых вещества: белый фосфор и красный фосфор.
Белый фосфор имеет молекулярную кристаллическую решетку, состоящую из молекул Р4. Нерастворим в воде, хорошо растворяется в сероуглероде. На воздухе легко окисляется, а в порошкообразном состоянии даже воспламеняется.
Белый фосфор очень ядовит. Особым свойством его является способность светиться в темноте вследствие его окисления. Хранят его под водой.
Красный фосфор представляет собой темно-малиновый порошок. Не растворяется ни в воде, ни в сероуглероде. На воздухе окисляется медленно и не самовоспламеняется. Неядовит и не светится в темноте.
При нагревании красного фосфора в пробирке, закрытой ватным тампоном, он превращается в белый фосфор (концентрированные пары), и если выдернуть тампон, белый фосфор вспыхнет на воздухе (рис. 35). Этот опыт показывает огнеопасность белого фосфора.
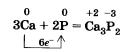
Химические свойства красного и белого фосфора близки, но белый фосфор более химически активен. Так, оба они, как и положено неметаллам, взаимодействуют с металлами, образуя фосфиды:
Белый фосфор самовоспламеняется на воздухе, а красный горит при поджигании. В обоих случаях образуется оксид фосфора^), выделяющийся в виде густого белого дыма:
4Р + 502 = 2Р205
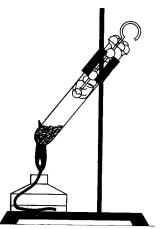
Рис. 35. Опыт, иллюстрирующий переход красного фосфора в белый
С водородом фосфор непосредственно не реагирует, фосфин РН3 можно получить косвенно, например из фосфидов:
Са3Р2 + 6НСl = ЗСаСl2 + 2РН3
Фосфин — очень ядовитый газ с неприятным запахом. Легко воспламеняется на воздухе. Это свойство фосфина и объясняет появление болотных блуждающих огней.
Соединения фосфора. При горении фосфина или фосфора образуется, как вы уже знаете, оксид фосфора Р205 — белый гигроскопичный порошок. Это типичный кислотный оксид, обладающий всеми свойствами кислотных оксидов.
Оксиду фосфора соответствует фосфорная кислота Н3Р04. Она представляет собой твердое прозрачное кристаллическое вещество, хорошо растворимое в воде в любых соотношениях. Как трехосновная кислота, Н3Р04 образует три ряда солей:
средние соли, или фосфаты, например Са3(Р04)2, которые нерастворимы в воде, кроме фосфатов щелочных металлов;
кислые соли — дигидрофосфаты, например Са(Н2Р04)2, большинство из которых хорошо растворимы в воде;
кислые соли — гидрофосфаты, например СаНР04, которые мало растворимы в воде (кроме фосфатов натрия, калия и аммония), т. е. занимают промежуточное положение между фосфатами и гидрофосфатами по растворимости.
В природе фосфор в свободном виде не встречается — только в виде соединений. Важнейшими природными соединениями фосфора являются минералы фосфориты и апатиты. Основную их массу составляет фосфат кальция Са3(Р04)2, из которого и получают в промышленности фосфор.
Биологическое значение фосфора. Фосфор является постоянной составной частью тканей организмов человека, животных и растений. В организме человека большая часть фосфора связана с кальцием. Для построения скелета ребенку требуется столько же фосфора, сколько и кальция. Кроме костей, фосфор содержится в нервной и мозговой тканях, крови, молоке. В растениях, как и у животных, фосфор входит в состав белков.
Из фосфора, поступающего в организм человека с пищей, главным образом с яйцами, мясом, молоком и хлебом, строится АТФ — аденозинтрифосфорная кислота, которая служит собирателем и носителем энергии, а также нуклеиновые кислоты — ДНК и РНК, осуществляющие передачу наследственных свойств организма. Наиболее интенсивно АТФ расходуется в активно работающих органах тела: в печени, мышцах, мозгу. Недаром знаменитый минералог, один из основоположников науки геохимии, академик А. Е. Ферсман назвал фосфор «элементом жизни и мысли».
Как было указано, фосфор существует в природе в виде соединений, содержащихся в почве (или растворенных в природных водах). Из почвы фосфор извлекается растениями, а животные получают фосфор с растительной пищей. После отмирания растительных и животных организмов фосфор снова переходит в почву. Так осуществляется круговорот фосфора в природе (рис. 36).
Применение фосфора и его соединений. Красный фосфор используют для производства спичек, фосфорной кислоты, которая, в свою очередь, идет на производство фосфорных удобрений и кормовых добавок для животноводства. Кроме того, фосфор применяют для получения ядохимикатов (вспомните баллончики с дихлофосом, хлорофосом и др.).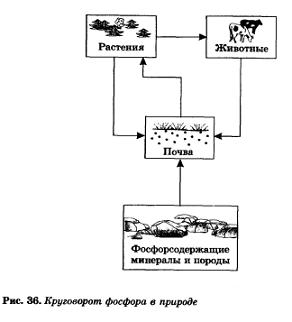
Открытие фосфора. Фосфор был открыт немецким алхимиком Г. Брандом в 1669 г. и получил свое название за его способность светиться в темноте (греч. фосфор — светоносный).
| Всего комментариев: 0 | |