| Главная » Статьи » 9 класс » Химия неметаллов |
| В категории материалов: 14 Показано материалов: 1-10 |
Страницы: 1 2 » |
Сортировать по: Дате · Названию · Рейтингу · Комментариям · Просмотрам
Азот
Строение и свойства атомов. Элемент азот N — первый представитель главной подгруппы V группы Периодической системы. Его атомы содержат на внешнем энергетическом уровне пять электронов, из которых три электрона неспаренные (вспомните правило «8-N»). Отсюда следует, что атомы этих элементов могут присоединять три электрона, завершая внешний энергетический уровень, и вследствие этого приобретают степень окисления -3, например в соединениях с водородом — аммиаке NН3 и с металлами — нитридах Li3N, Mg3N2 и др.
 NaaB4
NaaB4 Химия неметаллов
Химия неметаллов 0
0 1191
1191
Азотная кислота и ее соли
Азотная кислота и ее соли. Чистая HNO3 бесцветная жидкость, на воздухе «дымит», смешивается с водой. На свету частично разлагается, приобретая бурую окраску.
Получение.
1. В лаборатории азотную кислоту получают при взаимодействии безводных нитратов с концентрированной серной кислотой:
Ba (NO3)2 + H2SO4 → BaSO4↓ + 2HNO3.
 NaaB4
NaaB4 Химия неметаллов
Химия неметаллов 0
0 666
666
Аммиак и соли аммония
В лаборатории аммиак обычно получают, нагревая хлорид аммония  с гашеной известью
с гашеной известью  . Реакция выражается уравнением
. Реакция выражается уравнением
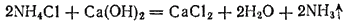
Выделяющийся аммиак содержит пары воды. Для осушения его пропускают через натронную известь (смесь извести с едким натром).
 NaaB4
NaaB4 Химия неметаллов
Химия неметаллов 0
0 2120
2120
Кислородсодержащие соединения галогенов
Степени окисления. Все галогены в галогенидных соединениях имеют степень окисления — 1. Такое состояние окисления для фтора в соединениях вообще является единственно возможным. Другие галогены могут существовать еще в состояниях с положительными степенями окисления. Эти состояния возникают в результате промотирования электронов с  -орбиталей атомов галогенов на их вакантные (незанятые электронами) d-орбитали (рис. 16.2). В атомах галогенов d-орбитали имеют сравнительно низкую энергию и поэтому оказываются легко доступными для заселения промотированными электронами.
-орбиталей атомов галогенов на их вакантные (незанятые электронами) d-орбитали (рис. 16.2). В атомах галогенов d-орбитали имеют сравнительно низкую энергию и поэтому оказываются легко доступными для заселения промотированными электронами.
 NaaB4
NaaB4 Химия неметаллов
Химия неметаллов 0
0 1114
1114
Кремний и его соединения. Стекло. Цемент
Кремний открыл и получил в 1823 году шведский химик Йенс Якоб Берцелиус.
Второй по распространённости элемент в земной коре после кислорода (27,6% по массе). Встречается в соединениях.
 NaaB4
NaaB4 Химия неметаллов
Химия неметаллов 0
0 1336
1336
Обобщение темы "Химия неметаллов"
Химические элементы-неметаллы.
Химические элементы, образующие простые вещества-неметаллы, располагаются в правом верхнем углу ПСХЭ Д.И. Менделеева. Таких химических элементов всего 16. Слева направо по периоду и снизу вверх по главной подгруппе радиусы атомов химических элементов уменьшаются, окислительные свойства и значения относительной электроотрицательности увеличиваются. Самый электроотрицательный элемент – фтор.
Особенностями строения атомов неметаллов по сравнению с металлами являются сравнительно небольшие атомные радиусы и большое число внешних электронов (как правило, 4 и более). Для большинства неметаллов будут более характерны окислительные свойства – им легче принимать электроны, чем отдавать.
 NaaB4
NaaB4 Химия неметаллов
Химия неметаллов 0
0 6224
6224
Оксиды азота
Оксид  , или закись азота,
, или закись азота,  получается при нагревании нитрата аммония:
получается при нагревании нитрата аммония:
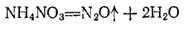
Оксид азота (I) представляет собою бесцветный газ со слабым запахом и сладковатым вкусом. Он мало растворим в воде: один объем воды при 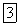 растворяет 0,63 объема
растворяет 0,63 объема  .
.
 NaaB4
NaaB4 Химия неметаллов
Химия неметаллов 0
0 1871
1871
Решение расчетных задач по теме "Неметаллы"
1. Задача 1
Расчеты по уравнению химической реакции с использованием правила об объемных отношениях газов:
Объемы реагирующих и получающихся газов (при одинаковых условиях) пропорциональны количествам этих веществ:
Задача №1. Какой объем хлороводорода может быть получен из 40 л хлора, если объемы газов измерены при одинаковых условиях?
 NaaB4
NaaB4 Химия неметаллов
Химия неметаллов 0
0 2409
2409
Свойства элементов и простых веществ галогенов
1. Свойства химических элементов галогенов
К галогенам относят фтор, хлор, бром, йод и астат. Они образуют VIIА-группу Периодической системы химических элементов.

Рис. 1. Химические элементы-галогены и образованные ими простые вещества
 NaaB4
NaaB4 Химия неметаллов
Химия неметаллов 0
0 1325
1325
Сероводород и сульфиды
Сероводород (H2S) – бесцветный газ с резким запахом гниющего белка. В природе встречается вводах минеральных ключей вулканических газах, гниении отбросов, а также при разложении белков погибших растений и животных.
Получение:
1) прямой синтез из элементов, при температуре 600 °C;
2) воздействием на сульфиды натрия и железа соляной кислотой.
Физические свойства: сероводород тяжелее воздуха, очень ядовит. Сжижение его происходит при -60,8 °C, затвердение – при -85,7 °C. Легко воспламеняется на воздухе. Растворим в воде – при температуре 20 °C в 1 литре воды можно растворить 2,5 литра сероводорода, при этом образуется сероводородная кислота.
 NaaB4
NaaB4 Химия неметаллов
Химия неметаллов 0
0 646
646