| Главная » Статьи » 10 класс » Непредельные углеводороды |
Алкадиены, каучук и резина
Строение алкадиенов
Алкадиены — ациклические углеводороды, содержащие в молекуле, помимо одинарных связей, две двойные связи между атомами углерода и соответствующие общей формуле СnН2n-2.
В зависимости от взаимного расположения двойных связей различают три вида диенов:
• алкадиены с кумулированным расположением двойных связей
СН2=С=СН2
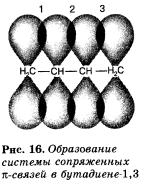
• алкадиены с сопряженными двойными связями
CH2=CH—CH=CH2
• алкадиены с изолированными двойными связями
CH2=CH—CH2—CH=CH2
Эти три вида алкадиенов существенно отличаются друг от друга по строению и свойствам. Центральный атом углерода (атом, образующий две двойные связи) в алкадиенах с кумулированными связями находится в состоянии ер-гибридизации. Он образует две Þ-связи, лежащие на одной прямой и направленные в противоположные стороны, и две я-связи, лежащие в перпендикулярных плоскостях.п-Связи образуются за счет негибридизованных р-орбиталей каждого атома углерода.
Свойства алкадиенов с изолированными двойными связями практически ничем не отличаются от свойств алкенов, разве что алкадиены вступают в соответствующие реакции в две ступени. Атомы углерода, образующие двойные связи, находятся в sр2-гибридизации.
Свойства алкадиенов с сопряженными связями весьма специфичны, так как сопряженные л-связи существенно влияют друг на друга.
р-Орбитали, образующие сопряженные п-связи, фактически составляют единую систему (ее называют п-системой), так как р-орбитали соседних л-связей частично перекрываются.
Длины двойных связей (1 и 3) составляют 0,137 нм (двойная связь в алкенах — 0,132 нм), а одинарной (2) — 0,146 нм (0,154 нм у алканов). Таким образом, можно считать, что кратность связей 1 и 3 несколько меньше двух, а связи 2 больше единицы.
Иногда алкадиены с сопряженными связями изображают следующим образом:
СН2—СН—СН—СН2
Изомерия и номенклатура
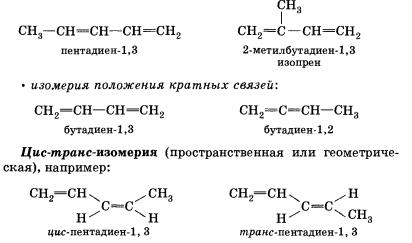
Для алкадиенов характерна как структурная изомерия, так и цис-транс-изомерия. Структурная изомерия:
• изомерия углеродного скелета:
Алкадиены изомерны соединениям классов алкинов и цик-лоалкенов (см. «Алкины»).
При формировании названия алкадиена указывают номера двойных связей. Главная цепь должна обязательно содержать обе кратные связи.
Получение
1. Метод Лебедева. В 1932 г. в нашей стране было налажено производство бутадиена из этилового спирта методом, разработанным С. В. Лебедевым. В основе метода лежит реакция
425 °С, Аl2O3, ZnO
2СН3—СН2—ОН -----------------> СН9=СН-СН=СН9 + 2Н2O + Н2
Серге́й Васи́льевич Ле́бедев
(1874-1934)
Советский химик, академик. Основные научные исследования посвящены полимеризации, изомеризации и гидрогенизации непредельных углеводородов. Получил (1928) синтетический каучук полимеризацией 1,3-бутадиена под действием натрия.
Этиловый спирт одновременно претерпевает и дегидратацию, и дегидрирование.
2. Способ дегидрирования. Одним из самых распространенных способов получения бутадиена-1,3 является двухстадий-ное каталитическое дегидрирование н-бутана:
СН3—СН2—СН2—СН3 —> CH2=CH—СН=СН2 + 2Н2
На первой стадии этого процесса образуется как бутен-1, так и бутен-2.
Не менее важное, чем бутадиен-1,3, другое соединение — изопрен (2-метилбутадиен-1,3) получают аналогичным способом — дегидрированием 2-метилбутана.
3. Способ дегидрогалогенирования. Для получения алкадиенов можно применять стандартный способ создания кратных связей — дегидрогалогенирование, известное вам еще по теме «Алкены».
При действии на дибромалканы спиртового раствора щелочи происходит отщепление двух молекул галогеноводорода и образование двух двойных связей: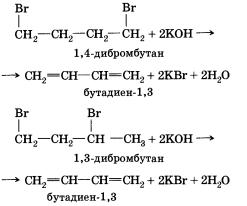
Существенным является расположение галогенов в молекуле дига-логенида. Так, например, в случае 2,3-дибромбутана или 2,2-ди-бромпропана образуются соответствующие алкины (см. § 13 «Алкины»).
Физические свойства
В обычных условиях пропадиен-1,2, бутадиен-1,3 — газы, 2-метилбутадиен-1,3 — летучая жидкость. Алкадиены с изолированными двойными связями (простейший из них — пен-тадиен-1,4) — жидкости. Высшие диены — твердые вещества.
Химические свойства
Напомним, что свойства алкадиенов с изолированными двойными связями мало отличаются от свойств алкенов. Алкадиены с сопряженными связями обладают некоторыми особенностями.
1. Реакции присоединения. Алкадиены способны присоединять водород, галогены, галогеноводороды.
Особенностью присоединения к алкадиенам с сопряженными двойными связями является способность присоединять молекулы как в положения 1 и 2 (1,2-присоединение), так и в положения 1 и 4 (1,4-присоединение):
Вr Вr
| |
СН2=СН—СН=СН2 + Вг2 —> CH2—CH—CH=CH2
1,2-присоединение
Вг Вг
| l
CH2=CH—СН=СН2 + Вг2 —> CH2—CH=CH—CH2
1,4-присоединение
Соотношение продуктов зависит от условий и способа проведения соответствующих реакций.
2. Реакции полимеризации. Важнейшим свойством диенов является способность полимеризоваться под воздействием катионов или свободных радикалов. Полимеризация этих соединений является основой получения синтетических каучуков. Обратите внимание на то, что полимеризация сопряженных диенов протекает как 1,4-присоединение.
В этом случае двойная связь оказывается центральной в элементарном звене, а элементарное звено, в свою очередь, может принимать как цис-, так и тракс-конфигурацию:
Рассмотрим причины, по которым в случае алкадиенов с сопряженными двойными связями возможно 1,4-присоединение на примере реакции гидробромирования (присоединения НВr).
Эта реакция протекает по механизму электрофильного присоединения и начинается с присоединения электрофильной частицы, катиона водорода, к молекуле алкадиена:
СН2=СН—СН=СН2 + H+ —> СН3—СН+—СН=СН2
Присоединение к этому карбокатиону иона Вr- приведет к продукту 1,2-присоединения:
СН3—СН+—СН=СН2 + Вr- —> СН3—СНВг—СН=СН2
Положительный заряд на атоме углерода означает наличие незаполненной р-орбитали, которая может перекрываться с л-связью, перетягивая к себе электронную плотность. В результате этого происходит перемещение двойной связи в центр молекулы, а положительный заряд оказывается на крайнем атоме углерода:
СН3—СН+—СН=СН2 —> CH3- СН=СН—СН2+
Обратите внимание на то, что мы встретились со случаем, когда одна и та же частица описывается двумя различными структурами, отличающимися друг от друга распределением электронной плотности. Присоединение аниона брома ко второму карбокатиону приведет к продукту 1,4-присоединения:
СН3—СН=СН—СН+ + Вг- —> СН3—СН=СН—СН2Вr
Натуральный и синтетический каучуки. Резина
До конца 1930-х гг. в промышленности использовали натуральный каучук, выделяемый из млечного сока (латекса) некоторых растений-каучуконосов. Наиболее ценным каучуконосом является гевея, растущая в Латинской Америке. Исследования показали, что натуральный каучук представляет собой цис-полиизопрен, т. е. полимер, элементарные звенья которого соответствуют изопрену (2-метилбутадиену-1,3) и находятся в цис-конфигурации.
Каучук, в котором все элементарные звенья находятся или в цис-, или в транс-конфигурации, называется стереорегулярным.
В середине прошлого века (Гудьир, 1839 г.) было обнаружено, что при нагревании каучука с серой (до 8%) образуется резина — эластичный материал, технические свойства которого гораздо лучше, чем у каучука. При нагревании с серой (вулканизации) происходит сшивание полимерных цепей за счет сульфидных мостиков, что приводит к увеличению прочности, устойчивости к истиранию, к действию органических растворителей и других веществ.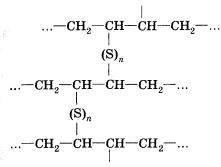
В связи с бурным ростом промышленного производства в начале XX в. возросла потребность в каучуке. И это заставило химиков искать пути получения синтетического каучука. Первые попытки были неудачными, так как при полимеризации диенов образовывались нестереорегулярные цепи (т. е. цепи, в которых элементарные звенья находились как в цис-, так и в траке-конфигурации). Получаемый каучук был похож на смолу, вулканизация его давала резину очень плохого качества.
Впервые технологически удобный способ синтеза полибутадиенового каучука был разработан русским химиком С. В. Лебедевым. В его основе лежала полимеризация бутадиена-1,3 с использованием катализатора — металлического натрия.
Это позволило получить полибутадиен с хорошими технологическими свойствами. Однако этот полимер был нестерео-регулярным, и поэтому резина, полученная на его основе, была менее эластичной, чем резина природного каучука. Стерео-регулярные полимеры (в том числе и изопреновые) научились получать лишь в 50-е гг. XX в.
Современная химическая промышленность вырабатывает несколько видов синтетического каучука. В качестве мономеров используют изопрен, бутадиен, хлоропрен (2-хлорбутадиен-1,3), стирол (винилбензол) и т. д. Большое распространение получили резины, произведенные на основе сополимеров алкадиенов с сопряженными двойными связями и производных алкенов.
Такие резины характеризуются высокой морозоустойчивостью, прочностью и эластичностью (бутадиен-стирольный), масло-бензостойкостью (бутадиен-нитрильный (нитрил — СН2=СН—СH)), пониженной газопроницаемостью, устойчивостью к действию ультрафиолетового излучения, окислителей (бутилкаучук — сополимер изопрена и изобутилена).
| Всего комментариев: 0 | |