| Главная » Статьи » 10 класс » Карбонильные соединения. Карбоновые кислоты |
Карбоновые кислоты. Строение, физические свойства, номенклатура
Карбоновыми кислотами называются соединения, содержащие карбоксильную группу
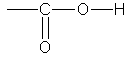
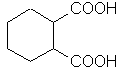
Классификация. По числу карбоксильных групп карбоновые кислоты делят на монокарбоновые, или одноосновные (одна группа -СООН), дикарбоновые, или двухосновные (две группы -СООН) и т.д. В зависимости от строения углеводородного радикала, с которым связана карбоксильная группа, карбоновые кислоты бывают алифатическими (например, уксусная или акриловая), алициклическими (например, циклогексанкарбоновая) или ароматическими (бензойная, фталевая). В таблице указаны некоторые представители карбоновых кислот.
Формула | Систематическое Название | Тривиальное Название |
Монокарбоновые кислоты | ||
HCOOH | метановая | муравьиная |
CH3COOH | этановая | уксусная |
C2H5COOH | пропановая | пропионовая |
C6H5COOH | бензойная | - |
CH3(CH2)16COOH | октадециловая | стеариновая |
CH2=CH-COOH | пропеновая | акриловая |
Дикарбоновые кислоты | ||
HOOC-COOH | этандиовая | щавелевая |
HOOC-CH2-COOH | пропандиовая | малоновая |
HOOC-CH2CH2-COOH | бутандиовая | янтарная |
| бензол-1,2- дикарбоновая | фталевая |
| бензол-1,4- дикарбоновая | терефталевая |
Если в углеводородном радикале карбоновых кислот атом (атомы) водорода замещен на другие функциональные группы, то такие кислоты называются гетерофункционапьными. Среди них различают галогенкарбоновые (например, CH2Cl—COOH), нитро-кислоты (например, NO2—С6Н4СООН), аминокислоты, оксикислоты (например, молочная СН3—СН(ОН)—СООН) и др.
Карбоновые кислоты с числом атомов углерода выше 6 называют высшими (жирными) кислотами. Название "жирные" эти кислоты получили потому, что большинство из них могут быть выделены из жиров.
Строение. Карбоксильная группа СООН состоит из карбонильной группы С=О и гидроксильной группы ОН. Свойства карбоксильной группы отличаются от свойств составляющих ее групп, которые оказывают взаимное влияние друг на друга. В группе СО атом углерода несет частичный положительный заряд и притягивает к себе неподеленную электронную пару атома кислорода в группе ОН. При этом электронная плотность на атоме кислорода уменьшается, и связь О-Н ослабляется:
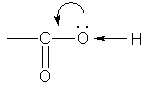
В свою очередь, группа ОН "гасит" положительный заряд на группе СО, которая из-за этого теряет способность к реакциям присоединения, характерным для карбонильных соединений.
Полезно подчеркнуть следующее важное обстоятельство, часто ускользающее от внимания читателей: карбоновые кислоты не единственный (хотя и самый многочисленный) класс органических веществ, обладающих кислотными свойствами. Очень сильными органическими кислотами являются сульфокислоты — органические соединения, содержащие сульфогруппу -SО3Н (например, метансульфокислота СН3SО3Н). Особенно важное значение имеют сульфокислоты ароматического ряда и их производные. Они являются промежуточными продуктами для синтеза различных органических веществ ( например, получение фенолов из сульфокислот ).
Номенклатура. В основе названий карбоновых кислот лежат названия соответствующих углеводородов. Наличие карбоксильной группы отражается окончанием -овая кислота. Низшие карбоновые кислоты часто имеют тривиальные названия: муравьиная, уксусная, масляная и др.
Углеводородную цепь нумеруют начиная с атома углерода карбоксильной группы, например:
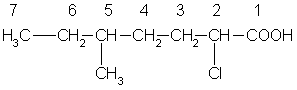
2-хлор-5-метилгептановая кислота
CH3—CH=CH—COOH
бутен-2-овая кислота
Часто карбоксильную группу рассматривают как заместитель в молекуле углеводорода. При этом в названии употребляют словосочетание "карбоновая кислота" и в нумерацию атомов углерода цепи атом углерода карбоксильной группы не включают:
9 8
СН3(СН2)7СН=СН(СН2)7СООН
Гептадецен-8-карбоновая (олеиновая) кислота
Названия дикарбоновых кислот производят от названия соответствующего углеводорода с добавлением суффикса "диовая" и слова "кислота". Например, этандиовая (щавелевая) кислота (НООС-СООН).
При рассмотрении карбоксильной группы как заместителя, название двухосновной кислоты производят от названия углеводородного радикала с добавлением словосочетания "дикарбоновая кислота". Например, малоновую кислоту (НООС-СН2-СООН) называют метандикарбоновой кислотой.
Физические свойства. Водородные связи (прочнее, чем у молекул спиртов!)
1. температуры кипения и плавления карбоновых кислот намного выше, не только чем у соответствующих углеводородов, но и чем у спиртов;
2. хорошая растворимость в воде (с увеличением углеводородного радикала уменьшается).
Водородные связи в карбоновых кислотах настолько сильны, что эти вещества образуют димеры:

Почему водородные связи между молекулами карбоновых кислот прочнее, чем между молекулами спиртов?
Потому что в карбоксильной группе выше положительный заряд на атоме водорода в гидроксиле: электроотрицательный атом кислорода карбонильной группы стягивает электронную плотность с гидроксильной группы.
Температуры плавления и кипения
Почему температура кипения разветвленного изомера бутановой кислоты ниже, чем изомера нормального строения?
Разветвленный углеводородный радикал подает на карбоксильную группу большую электронную плотность, чем неразветвленный, и полярность связи О- Н уменьшается по сравнению с изомером нормального строения.
Почему температуры плавления изменяются зигзагообразно?

Растворимость

На переход из твердого состояния в жидкое (разрушение кристалла) влияет не только сила межмолекулярного взаимодействия, но еще и способ упаковки молекул в кристаллической решетке. От числа (четности) атомов углерода в молекуле зависит, под каким углом друг к другу будут расположены карбоксильные группы в кристалле. В зависимости от этого между молекулами образуются две или одна водородная связь, а это очень сильно влияет на прочность кристалла.
Кислоты, содержащие более 10 атомов углерода, можно считать нерастворимыми.
| Всего комментариев: 0 | |